QS Informa Voltar NOTÍCIA ANVISA!
Última atualização: 05 de novembro de 2020 9:53 pm
NOTÍCIA ANVISA!
Agência brasileira aprova antidepressivo na forma de spray inalável.
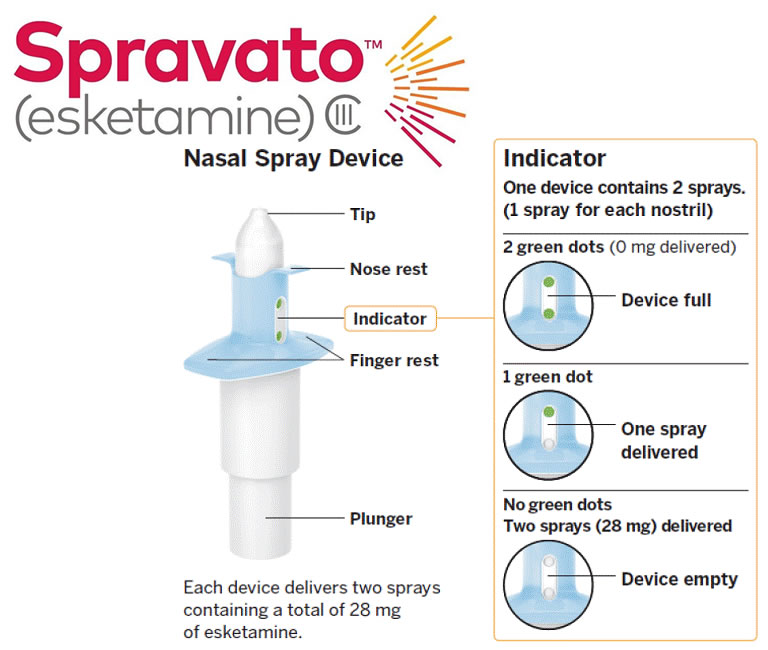
A Agência Nacional de Vigilância Sanitária aprovou, nesta terça-feira (03/11), o cloridrato de escetamina, um antidepressivo na forma de spray inalável indicado para adultos com depressão resistente a tratamentos convencionais e para pessoas com transtorno depressivo maior (TDM) que tenham pensamentos ou atos suicidas. O novo medicamento, chamado SPRAVATO (desenvolvido pela Janssen, divisão farmacêutica da Johnson & Johnson), segundo a Anvisa, deverá ser administrado exclusivamente em um hospital ou uma clínica especializada e na presença de um profissional da saúde. O remédio tem como base a escetamina (ou esketamina). O princípio ativo tem relação com a cetamina (ou ketamina), um medicamento usado para anestesias.
O medicamento é apresentado como o primeiro a agir sobre o glutamato, molécula da rede neural, estimulando áreas do cérebro ligadas às emoções, enquanto os antidepressivos tradicionais atuam aumentando a quantidade de neurotransmissores relacionados à sensação de prazer e bem-estar. Apesar de ser uma forma inovadora, o tratamento deve ser administrado também com um antidepressivo oral.
Os testes de fase três para a aprovação da medicação demonstraram que a escetamina em conjunto com os medicamentos orais foi responsável por uma redução nos sintomas depressivos em até 24 horas após a administração da primeira dose. A Anvisa afirma em nota que “o medicamento tem demonstrado rápido início de ação com perfil risco-benefício-favorável e tolerabilidade do paciente ao tratamento”.
A depressão é uma doença que afeta cerca de 264 milhões de pessoas no mundo, segundo levantamento da Organização Mundial da Saúde (OMS) datado de janeiro de 2020. Ainda segundo a OMS, quase 800.000 pessoas morrem devido ao suicídio todos os anos. O suicídio é a segunda principal causa de morte entre jovens de 15 a 29 anos. As mulheres são mais afetadas pela depressão do que os homens. Segundo estudo do NIMH (National Institute of Mental Health-USA), estima-se que 17,3 milhões de adultos nos Estados Unidos tiveram pelo menos um episódio de depressão, número este que representa 7,1% de todos os adultos dos EUA. A prevalência de episódio depressivo foi maior entre mulheres adultas (8,7%) em comparação com homens (5,3%). A prevalência de adultos com episódio depressivo maior foi maior entre os indivíduos de 18 a 25 anos (13,1%). Já no Brasil, mais de 10 milhões de pessoas apresentam sinais de depressão, o que faz com que o país tenha a maior incidência da doença na América Latina.
Spravato já é aprovado nos EUA (desde março de 2019) e na Europa (desde dezembro de 2019). Segundo o FDA, o rótulo do Spravato contém uma caixa de advertência que alerta que os pacientes estão sob risco de sedação e dificuldade de atenção, julgamento e raciocínio (dissociação), abuso e uso indevido e pensamentos e comportamentos suicidas após a administração do medicamento. Devido ao risco de sedação e dissociação, os pacientes devem ser monitorados por um profissional de saúde por pelo menos duas horas após receber a dose do medicamento. O REMS (Risk Evaluation and Mitigation Strategy) exige que o prescritor e o paciente assinem um “Formulário de Inscrição do Paciente”, afirmando claramente que o paciente entende que deve tomar providências para deixar o ambiente de saúde com segurança para chegar em casa e que o paciente não deve dirigir ou usar máquinas pesadas para o resto do dia. Os principais efeitos colaterais observados durante a administração do medicamento foram dissociação, tontura, náusea, sedação, visão embaçada, sentido reduzido de toque e sensação, ansiedade, falta de energia, pressão arterial elevada, vômito, parestesia e sensação de embriaguez. O resultado a longo prazo indica que, apesar disso, 51% dos pacientes tiveram queda nos riscos de recaída usando o tratamento intranasal, uma vez a cada duas semanas, se comparados com aqueles que deixaram de fazer o tratamento continuado.
Fontes: Globo, Exame, FDA, NIMH, WHO